統括管理者は、自身の研究に関する医薬品等製造販売業者等(関係企業等)を抽出し、関係性を整理して利益相反状況を管理する必要があります。また、その手順については、標準的な利益相反管理の手順が厚生労働省から提示されております。
| ▶ 「臨床研究法における利益相反管理について」 |
| <クリックすると記載場所に移動できます>
1. 利益相反状況の確認時期 |
1. 利益相反状況の確認時期
2. 利益相反状況の確認時に必要な書類
| 書類名 | 備考 |
|---|---|
| 利益相反状況確認依頼書 (特定様式1)*¹ |
<書類> こちらからダウンロード可能です。 <様式C> 利益相反申告者*²の人数分必要です。 |
| 研究分担医師リスト (統一書式1) |
|
| 利益相反管理様式(様式A~E、X) | |
| 研究計画書 | 最新版の研究計画書、説明文書・同意文書をご提出ください。 ※新規申請の場合はドラフト版を提出 |
| 説明文書・同意文書 |
※1 利益相反状況確認依頼書(特定様式1)
・本学の利益相反状況確認依頼の際に作成・提出が必要となる学内様式です。
※2 利益相反申告者とは
・統括管理者
・研究責任医師
・研究分担医師
・統計解析責任者
・臨床研究を実施することによって利益を得ることが明白な者
・医学に関する知識に基づく必要な助言を求めることができる者
3. 利益相反管理様式の作成方法
・厚生労働省「臨床研究法における利益相反管理について」の手順に基づき
・作成された、Excel形式の様式です。
・統括管理者は、本様式を用いて利益相反状況を確認し、作成した様式Aと
・様式Eを認定臨床研究審査委員会に提出します。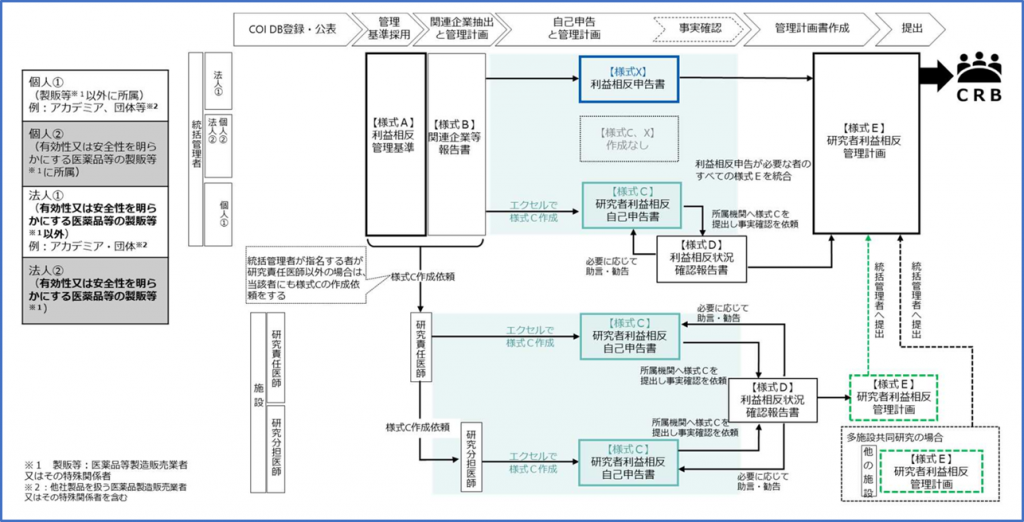 (画像出典:厚生労働省「臨床研究法における臨床研究の利益相反管理について」)
(画像出典:厚生労働省「臨床研究法における臨床研究の利益相反管理について」)
※画像をクリックすると、拡大版が表示されます。
※本学の利益相反管理フローはこちらをご確認ください。
(「学校法人日本医科大学における特定臨床研究の利益相反状況確認に関する手順書」抜粋)
| 様式名 | 内容 | ||
|---|---|---|---|
| 様式A 利益相反 管理基準 |
臨床研究と関わりのある企業等との利益相反の状態を 適切に管理するための基準を策定する。 |
||
| 様式B 関係企業等 報告書 |
臨床研究への企業等の関与の有無を判定し、 利益相反管理基準に則って管理計画を立てる。 |
||
| 様式C 研究者利益相反 自己申告書 |
様式Bで抽出した関係企業等と研究者との間の個人的利益関係 の有無を確認し、自身の利益相反状況を自己申告する。 (奨学寄附金の受領や個人的利益の有無等) ※<統括管理者、研究責任医師用> <研究分担医師等用> |
||
| 様式D 利益相反状況 確認報告書 |
実施医療機関等で把握している情報と様式Cの内容が合致して いるか事実確認を行い、所属機関の管理者が確認報告書を 作成し、研究責任医師に送付する。 |
||
| 様式E 利益相反 管理計画 |
臨床研究と関わりのある企業等との利益相反の状態と 当該利益相反に対する管理計画をまとめ、 認定臨床研究審査委員会に提出し意見を聴取する。 |
||
※1 様式Cは利益相反申告者一人一人が作成する必要があるため、研究責任
※1医師は、自身の所属機関の利益相反申告者全員に様式Cの作成を依頼して※1ください。
※2 統括管理者、研究責任医師は動画1・資料1を参照してください。
※2研究分担医師等は動画2・資料2を参照してください。
※3 作成した様式Eは統括管理者に提出してください。
※4 様式AからEの作成方法の詳細についてはこちらをご覧ください。
4. 利益相反状況確認依頼書の作成方法
・利益相反の確認依頼時期ごとの記載例を参考にして作成してください。
・作成方法については、 3.利益相反管理様式の作成方法 の
・《各様式の作成者および作成方法》「様式D作成依頼」にある動画・資料も
・合わせてご確認ください。
| 利益相反確認依頼が必要となるとき | 記載例 | 区分 | |
|---|---|---|---|
| 研究の開始 | 研究開始前 | 例1 | 新規 |
| 実施中の研究に研究分担施設として新たに参加 | 例2 | 変更 | |
| 利益相反 申告者の 変更 |
実施医療機関(自施設)の統括管理者の変更 実施医療機関(自施設)の研究責任医師の変更 実施医療機関(自施設)の研究分担医師の追加 |
例3 | |
| 利益相反 申告事項の 変更 |
関連企業の追加 | 例4 | |
| 資金源の変更 | 例5 | ||
| その他 (個⼈的利益、企業役員就任、株式取得、特許出願 等) |
|||
| 定期報告 | jRCT(臨床研究等提出・公開システム)の 初回公表日から起算して1年ごと |
例6 | 定期報告 |
| その他 | 統括管理者(又は研究代表事務局)の求めに応じて | その他 | |
・利益相反状況の確認依頼時期と記載例のまとめはこちらをご覧ください。
5. 利益相反状況の確認依頼先(所属担当部署)
各所属機関にて利益相反状況の確認依頼の窓口は以下の通りです。
研究責任医師は、 2.利益相反状況の確認時に提出する書類に記載の書類を用意し、部署長の承諾を得た後、所属担当部署に書類を提出してください。
6. 定期報告時の利益相反状況確認の簡略化
定期報告時に限り、以下の条件がすべて満たされる場合、利益相反状況確認の一部プロセスを簡略化することができます。
▶詳細は こちら
◇ お問い合わせ先
-
- 学校法人日本医科大学 臨床研究審査委員会事務局
- E-mail:officetokutei★nms.ac.jp
(★を@にしてご利用ください) - TEL :03-3822-2131(内線5915,5921)
- FAX :03-3868-9159
- ADD :〒113-8602 東京都文京区千駄木1-1-5



